O p53 é um dos principais reguladores da estabilidade genômica, atuando no controle do ciclo celular, na indução de apoptose e na resposta ao dano do DNA. Alterações nesse eixo estão entre os eventos mais comuns na carcinogênese, e mutações no TP53 estão presentes em quase 50% dos tumores sólidos, configurando o gene mais frequentemente alterado no câncer humano.1 Entre essas alterações, a mutação TP53 Y220C corresponde a cerca de 2% de todos os cânceres com mutação de p53, com distribuição em diferentes histologias.2,3 Diferentemente da maioria das mutações do p53, que levam apenas à perda de função, a Y220C gera uma cavidade estrutural específica na proteína, criando uma vulnerabilidade biológica potencialmente explorável do ponto de vista terapêutico.4
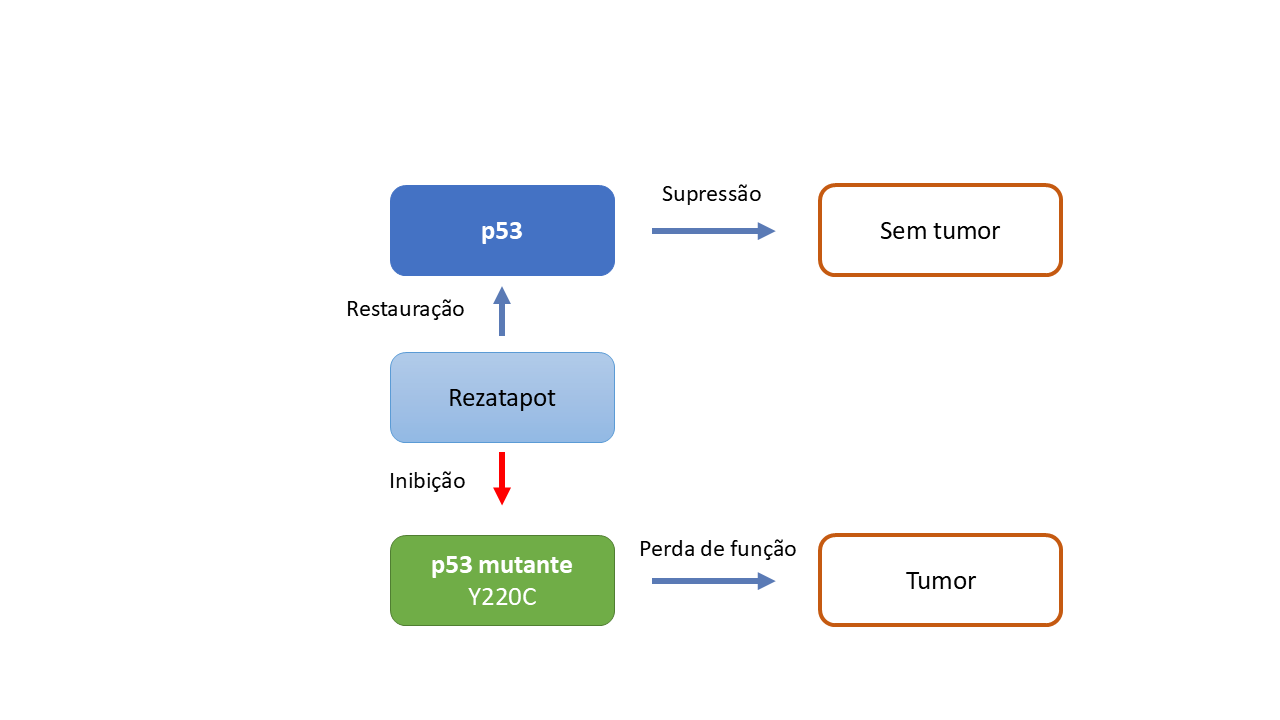
A partir dessa alteração estrutural, foi desenvolvido pela empresa PMV Pharmaceutical o rezatapopt (PC14586), uma pequena molécula desenhada para se ligar seletivamente a essa cavidade e estabilizar o p53 mutante em uma conformação funcional.4 Ao fazer isso, o fármaco permite recuperar parcialmente a atividade supressora tumoral da proteína. Essa estratégia representa uma mudança conceitual relevante, ao propor não o bloqueio de vias oncogênicas, mas a restauração de uma função biológica perdida, explorando uma característica estrutural específica da mutação.
Os primeiros dados clínicos dessa abordagem foram avaliados em um estudo com 77 pacientes com tumores sólidos avançados portadores da mutação TP53 Y220C, previamente tratados com múltiplas linhas de tratamento. A população incluiu principalmente câncer de ovário, mama, pâncreas e colorretal. O tratamento apresentou perfil de segurança manejável, com eventos adversos mais frequentes como náuseas (58%), vômitos (44%), fadiga (39%) e anemia (36%), sendo anemia grau ≥3 observada em 15% dos pacientes, e taxa de descontinuação de 8%, sem mortes relacionadas ao tratamento.5 Do ponto de vista de eficácia, observou-se taxa de resposta objetiva de 20%, com respostas em diferentes tumores, especialmente em ovário e mama, e duração mediana de resposta de 7,0 meses (IC de 95%, 2,8–10,6) (4). Um achado relevante foi a influência do contexto molecular, uma vez que todos os pacientes respondedores apresentavam KRAS sem mutação, e, nesse subgrupo, a taxa de resposta alcançou 30%, sugerindo que a eficácia da reativação do p53 depende do equilíbrio entre diferentes vias oncogênicas no tumor.5 Do ponto de vista clínico e translacional, esses resultados representam a primeira demonstração consistente de que a reativação farmacológica de uma proteína supressora tumoral mutante pode gerar benefício clínico mensurável. Ao mesmo tempo, dados recentes indicam que o uso do tratamento pode favorecer o surgimento de mutações secundárias no próprio TP53, associadas ao desenvolvimento de resistência adquirida .3 Nesse contexto, o rezatapopt ainda se encontra em desenvolvimento, mas seus resultados indicam que alterações estruturais específicas do p53 podem ser abordadas de forma terapêutica. Esse racional também sustenta o avanço de estratégias voltadas à restauração funcional de proteínas, possivelmente associadas a tratamentos combinados para reduzir o risco de resistência tumoral. Referências: 1. Kandoth C, et al. Nature. 2013; 502(7471):333-339. 2. Joerger AC, Fersht AR. Annu Rev Biochem. 2016; 85:375-404. 3. Fece de la Cruz F, el al. Cancer Discov. 2026; 16(4):677-685. 4. Wang W. Signal Transduct Target Ther. 2026;11(1):121. 5. Dumbrava EE. N Engl J Med. 2026; 394(9):872-883.4.

Os primeiros dados clínicos dessa abordagem foram avaliados em um estudo com 77 pacientes com tumores sólidos avançados portadores da mutação TP53 Y220C, previamente tratados com múltiplas linhas de tratamento. A população incluiu principalmente câncer de ovário, mama, pâncreas e colorretal. O tratamento apresentou perfil de segurança manejável, com eventos adversos mais frequentes como náuseas (58%), vômitos (44%), fadiga (39%) e anemia (36%), sendo anemia grau ≥3 observada em 15% dos pacientes, e taxa de descontinuação de 8%, sem mortes relacionadas ao tratamento.5 Do ponto de vista de eficácia, observou-se taxa de resposta objetiva de 20%, com respostas em diferentes tumores, especialmente em ovário e mama, e duração mediana de resposta de 7,0 meses (IC de 95%, 2,8–10,6) (4). Um achado relevante foi a influência do contexto molecular, uma vez que todos os pacientes respondedores apresentavam KRAS sem mutação, e, nesse subgrupo, a taxa de resposta alcançou 30%, sugerindo que a eficácia da reativação do p53 depende do equilíbrio entre diferentes vias oncogênicas no tumor.5 Do ponto de vista clínico e translacional, esses resultados representam a primeira demonstração consistente de que a reativação farmacológica de uma proteína supressora tumoral mutante pode gerar benefício clínico mensurável. Ao mesmo tempo, dados recentes indicam que o uso do tratamento pode favorecer o surgimento de mutações secundárias no próprio TP53, associadas ao desenvolvimento de resistência adquirida .3 Nesse contexto, o rezatapopt ainda se encontra em desenvolvimento, mas seus resultados indicam que alterações estruturais específicas do p53 podem ser abordadas de forma terapêutica. Esse racional também sustenta o avanço de estratégias voltadas à restauração funcional de proteínas, possivelmente associadas a tratamentos combinados para reduzir o risco de resistência tumoral. Referências: 1. Kandoth C, et al. Nature. 2013; 502(7471):333-339. 2. Joerger AC, Fersht AR. Annu Rev Biochem. 2016; 85:375-404. 3. Fece de la Cruz F, el al. Cancer Discov. 2026; 16(4):677-685. 4. Wang W. Signal Transduct Target Ther. 2026;11(1):121. 5. Dumbrava EE. N Engl J Med. 2026; 394(9):872-883.4.
Últimas notícias
FDA aprova o primeiro PROTAC oncológico para o tratamento do câncer de mama avançado co...
5 de maio de 2026
/3 min. de leitura
Nivolumabe em combinação com AVD é aprovado pela ANVISA como tratamento de primeira lin...
5 de maio de 2026
/4 min. de leitura
EVENTOS | Simpósio Internacional de Medicina de Precisão em Câncer Gastrointestinal
29 de abril de 2026
/1 min. de leitura
Atenção: O conteúdo deste site destina-se exclusivamente a profissionais de saúde. Nunca tome medicamentos tarjados por conta própria; siga sempre as orientações de seu médico. Os autores e editores desta obra fizeram todo esforço para assegurar que as doses e as indicações dos fármacos, bem como dos procedimentos apresentados no texto, estivessem de acordo com os padrões vigentes à época da publicação. Em virtude dos constantes avanços da Medicina e de possíveis modificações regulamentares referentes aos fármacos e procedimentos apresentados, recomendamos que o usuário consulte sempre outras fontes fidedignas, de modo a se certificar de que as informações contidas neste site estão corretas. Isso é particularmente importante no caso de fármacos ou procedimentos novos ou pouco usados. Este site, para uso exclusivo por profissionais de saúde, é editado com objetivos educacionais, estando em conformidade com a resolução no. 097/2001 do Conselho Regional de Medicina do Estado de São Paulo. Responsável técnico: Dr. Antonio Carlos Buzaid, CRM-SP 45405. Nenhuma parte pode ser reproduzida ou transmitida sem a autorização dos autores. O conteúdo deste site é produzido de forma independente e autônoma, sem qualquer interferência das empresas/instituições apoiadoras ou patrocinadoras e sem que haja qualquer obrigação por parte de seus profissionais em relação à recomendação ou prescrição dos produtos/serviços eventualmente comercializados por quaisquer dessas empresas/instituiçõesCopyright © 2026 Antonio Carlos Buzaid. Desenvolvimento: DENDRIX CNPJ 05.371.865/0001-88


